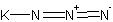выберите первую букву в названии статьи:
1-9
А Б В Г Д Е Ж З И К Л М Н О П Р С Т У Ф Х Ц Ч Ш Щ Э Ю Я
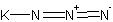
Внешний вид:
бесцветн. тетрагональные кристаллы
Кристаллические модификации, цвет растворов и паров:
Параметры терагональной модификации: a = 0,6094 нм, c = 0,7056 нм, z = 4, пространственная группа I4/mcm.
Брутто-формула (система Хилла): KN3
Формула в виде текста: KN3
Молекулярная масса (в а.е.м.): 81,12
Температура плавления (в °C): 354
Температура разложения (в °C): 360
Продукты термического разложения:
калий, азот
Растворимость (в г/100 г или характеристика):
аммиак жидкий: хорошо растворим
ацетон: не растворим
бензол: плохо растворим
вода: 41,4 (0°C)
вода: 46,5 (10,5°C)
вода: 48,9 (15,5°C)
вода: 49,6 (17°C)
вода: 105,7 (100°C)
диэтиловый эфир: плохо растворим
этанол: 0,16 (0°C)
этанол: 0,137 (16°C)
Вкус, запах, гигроскопичность:
не гигроскопичен
Метод получения 1.
(лабораторный синтез)
Источник информации: "Неорганические синтезы" сб.2 М.: ИИЛ 1951 стр. 136-137Сперва приготовляют раствор 65—70 г едкого кали в 500 мл абсолютного этилового спирта. Растворение при комнатной температуре проходит крайне медленно и потому смесь подогревают. Для осаждения нерастворимых в спирте примесей лучше применять высокий цилиндр, а затем декантировать чистый раствор в 1-литровую круглодонную колбу, соединенную с холодильником посредством стеклянного шлифа (примечание 1). К раствору добавляют 60 г (1 моль) технического 85-процентного раствора гидразингидрата (примечание 2). Смесь слегка подогревают на паровой бане и добавляют 15 г бутилнитрита в качестве затравки. Затем колбу с присоединенным к ней холодильником снимают с паровой бани и вводят дополнительно 110 г бутилнитрита (суммарное количество которого будет доведено таким образом до 125 г, или 1,2 моля) с такой скоростью, чтобы смесь слегка кипела. Обычно эта операция продолжается приблизительно 1 час. Затем колбу вновь нагревают на паровой бане в течение 15 минут для завершения реакции. Во время реакции из раствора выпадает азид калия. Колбу охлаждают в бане со льдом. Твердое вещество отфильтровывают, промывают четырьмя порциями по 50 мл холодного абсолютного этилового спирта, а затем двумя порциями абсолютного эфира (125 и 100 мл). Препарат сушат на воздухе при 55—60°. Выход 63—69 г (78—84%). Этот препарат оказывается достаточно чистым для большинства целей (98,9% KN3). Однако, в случае необходимости, его можно очистить путем растворения в воде и повторного осаждения добавлением этилового спирта. Еще 6—8 г азида калия, содержащего примеси, можно получить упариванием маточного раствора до 100 мл с последующим охлаждением и фильтрованием. Примечание 1. Если лаборатория не располагает цельностекляиной аппаратурой, пробковые и резиновые части следует покрывать оловяниой фольгой для предохранения их от корродирующего действия паров гидразина. Примечание 2. Если применяется 45-процентный гидразин, выход будет несколько меньшим и в растворе останется большее количество препарата.
Способы получения:
1. Получают взаимодействием оксида азота (I) с расплавленным амидом калия при 280 С.
2. Реакцией едкого кали с азотистоводородной кислотой.
Плотность:
2,056 (20°C, г/см3)
Стандартная энтальпия образования ΔH (298 К, кДж/моль):
-1,7 (т)
Стандартная энтропия образования S (298 К, Дж/моль·K):
104 (т)
Стандартная мольная теплоемкость Cp (298 К, Дж/моль·K):
76,9 (т)
История:
Впервые получен в 1898 г.
Дополнительная информация:
Хорошо растворяется в растворе бромистого калия. В жидком оксиде серы (IV) желтеет и взрывается. От удара не взрывается. Реагирует с иодом в присутствии сероуглерода с образованием иодида калия и азота. При слабом нагревании интенсивно реагирует с двуокисью марганца давая манганат калия и азот. Может быть использован для качественного и количественного анализа тория.
Источники информации:
- "Справочник химика" т.2, Л.-М.: Химия, 1964 стр. 80-81
- "Химическая энциклопедия" т.2 М.: Советская энциклопедия, 1990 стр. 285
- "Энергетические конденсированные системы" под ред. Жукова Б.П., 2-е изд. М.:Янус-К 2000 стр. 19
- Багал Л.И. "Химия и технология инициирующих взрывчатых веществ" М. 1975 стр. 158-159
выберите первую букву в названии статьи:
1-9
А Б В Г Д Е Ж З И К Л М Н О П Р С Т У Ф Х Ц Ч Ш Щ Э Ю Я
|