Хелат железа
Re: Хелат железа
Ув.stallker,в принципе Ваш метод более-менее ясен,но растениям нужно подать необходимый катион в лиганде,комплексом,т.к это предотвратит от многих негативных факторов,ожидающих ион металла в аквариумной воде,а именно-соединение в нерасстворимые соли-в основном фосфаты,различные ОВР и т.д.И самый главный момент-это потеря биодоступности,хелатор в данном случае выполняет роль транспортёра катиона к кутикулам растительной клетки,сглаживая острые углы на пути,а различие хелаторов-это преждевсего стабильность и устойчивость комплексов.Вот поэтому нужно создать комплексный расствор с хелатами железа и другими металлами. 
Re: Хелат железа
На комплексы так же могут оказывать влияние бактерии живужие в аквариуме:deps писал(а):И самый главный момент-это потеря биодоступности,хелатор в данном случае выполняет роль транспортёра катиона
http://www.vesti.ru/doc.html?id=1023568&cid=2161
Интересный момент с ионами серебра:
Работа учёных показала, что сами частицы в 7,5 тысяч раз менее токсичны для бактерий, чем ионы серебра. При этом исследователи установили, что в небольших концентрациях ионы могут оказывать обратный эффект на бактерии и, наоборот, стимулировать их развитие.
Сократ мне друг, но истина дороже.
Re: Хелат железа
однозначно,это давно доказано,что лучше хелатировать металлы синтетическими комплексообразователями (ЭДТА,ДТПА,ОЭДФ и т.д),а не карбо и аминокислотами,т.к такие комплексы более подвержены разрушающему действию бактерий.stallker писал(а):На комплексы так же могут оказывать влияние бактерии живужие в аквариуме:
Re: Хелат железа
Все простые соли из доступных уже перебрали. Остальные либо малорастворимы либо с токсичным анионом в составе.deps писал(а):...Может ещё посоветуете какие нибудь соли железа 3 ?Спасибо.
Странно. По идее природа аниона исходной соли не должна радикально сказываться на свойствах полученного комплекса. С самодельным сульфатом возможно это "шутки" избыточной перекиси, если на практике был избыток. Попробуйте погреть или даже прокипятить раствор после окисления железа до 3-х валентного.deps писал(а):...Вот сульфат не могу найти,сделал как Вы писали по реакции,добавил ОЭДФ-расствор стал коричнево-тёмного цвета и просветлел при нейтрализации аж в районе 10-11,а это неприемлимо для аквариума.Пока квасцы...
Сам в данный момент далеко от лаборатории и проверить в ближайшее время не смогу.
Бог на стороне не больших батальонов, а тех, кто лучше стреляет (приписывается Вольтеру)
Re: Хелат железа
Ув.amik,спасибо,попробую-отпишусь. 
Re: Хелат железа
Ув.amik,всё-таки не давал мне покоя состав ОЭДФ и солей железа 2  .В итоге решил попробовать заново,но немного другим путём.Взял расстворил навеску ОЭДФ-РН 2-2.5,и тут же не внося никакие соли,нейтрализовал кислый расствор ОЭДФ до РН 6 гидрокарбонатом калия.Затем внёс медный купорос и железный купорос-всё как и наблюдалось раннее-расствор резко побурел,но через некоторое время стал тёмно-зелёного,прямо с чернотой цвета (видимо эта окраска проявилась с РН 6,в кислом расстворе окраска была красно-бурой,тёмно-кирпичного цвета).Вот тут решил подумать и пришёл к логическому умозаключению (возможно не правильному!)
.В итоге решил попробовать заново,но немного другим путём.Взял расстворил навеску ОЭДФ-РН 2-2.5,и тут же не внося никакие соли,нейтрализовал кислый расствор ОЭДФ до РН 6 гидрокарбонатом калия.Затем внёс медный купорос и железный купорос-всё как и наблюдалось раннее-расствор резко побурел,но через некоторое время стал тёмно-зелёного,прямо с чернотой цвета (видимо эта окраска проявилась с РН 6,в кислом расстворе окраска была красно-бурой,тёмно-кирпичного цвета).Вот тут решил подумать и пришёл к логическому умозаключению (возможно не правильному!)  -если медь восстановилась,почему бы её не окислить? В этот тёмный расствор,содержащий медь,железо и ОЭДФ,влил немного перекиси водорода,результат-расствор моментально посветлел и стал светло-салатового цвета,РН 6
-если медь восстановилась,почему бы её не окислить? В этот тёмный расствор,содержащий медь,железо и ОЭДФ,влил немного перекиси водорода,результат-расствор моментально посветлел и стал светло-салатового цвета,РН 6  .Оставил немного постоять-никаких изменений.Затем провёл последовательное расстворение-хлорид марганца(вначале произошло небольшое хлопьеобразование,расствор потемнел и через некоторое время стал светло-коричневый,без хлопьев,осадков и т.д).Сульфат цинка-небольшие хлопья,просветление.Сульфаты никеля и кобальта-результат тот же,но расствор оставался светлым,но намечалась тенденция потемнения,НО без осадков и хлопьеобразования.Молибдат,ванадат-никаких изменений (раньше,как Вы помните,проявлялась интенсивно коричневая окраска при его внесении).Окончательный расствор прозрачный,коричневого цвета,РН в районе 5.5-6,т.е не требующий окончательной нейтрализации.Думаю,что применив перекись,вернул медь в 2 вал.состояние,но окислил железо 2 в 3,и в итоге получил комплекс не железо 2+ОЭДФ,а 3+ОЭДФ.Расствор остался без солей магния,учитывая его кол-во,боюсь изменить хим.состав готового пит.расствора.В последнюю очередь внёс борную кислоту-это не изменило ни цвет,ни РН,но появилось выделение газа (предположительно СО2 из гидрокарбоната калия).Интересно,что запах такого расствора стал не типично "железным",а какой-то карамельный (так пахнет сухой глюконат железа).
.Оставил немного постоять-никаких изменений.Затем провёл последовательное расстворение-хлорид марганца(вначале произошло небольшое хлопьеобразование,расствор потемнел и через некоторое время стал светло-коричневый,без хлопьев,осадков и т.д).Сульфат цинка-небольшие хлопья,просветление.Сульфаты никеля и кобальта-результат тот же,но расствор оставался светлым,но намечалась тенденция потемнения,НО без осадков и хлопьеобразования.Молибдат,ванадат-никаких изменений (раньше,как Вы помните,проявлялась интенсивно коричневая окраска при его внесении).Окончательный расствор прозрачный,коричневого цвета,РН в районе 5.5-6,т.е не требующий окончательной нейтрализации.Думаю,что применив перекись,вернул медь в 2 вал.состояние,но окислил железо 2 в 3,и в итоге получил комплекс не железо 2+ОЭДФ,а 3+ОЭДФ.Расствор остался без солей магния,учитывая его кол-во,боюсь изменить хим.состав готового пит.расствора.В последнюю очередь внёс борную кислоту-это не изменило ни цвет,ни РН,но появилось выделение газа (предположительно СО2 из гидрокарбоната калия).Интересно,что запах такого расствора стал не типично "железным",а какой-то карамельный (так пахнет сухой глюконат железа).
Написал много,дотошно,Вам конечно хватило бы пару предложений,но решил освятить более детально.Посему вопросы:
1.Имеет ли смысл такого соства?
2.Возможна ли его работоспособность на практике с хим. точки зрения?
3.Оправдано ли применение перекиси или другого окислителя? ну и так далее...
Написал много,дотошно,Вам конечно хватило бы пару предложений,но решил освятить более детально.Посему вопросы:
1.Имеет ли смысл такого соства?
2.Возможна ли его работоспособность на практике с хим. точки зрения?
3.Оправдано ли применение перекиси или другого окислителя? ну и так далее...
Re: Хелат железа
Интересный эксперимент и изложение наблюдений просто блеск 
Успехов
Думаю получается в результате то же самое - смесь комплексов, но меньшей кровью и без возни с изменением рН. Осталось проверить пригодность и работоспособность на реальных объектах, без этого никак. Наверно сразу рисковать большим аквариумом не стоит.deps писал(а):1.Имеет ли смысл такого соства?
2.Возможна ли его работоспособность на практике с хим. точки зрения?
Судя по наблюдающейся картине, очень даже помогает получить стабильный раствор. Не повлияет ли на растения и рыбок в аквариуме возможный небольшой избыток перекиси, поскольку ее разложение ингибируется переводом металлов - катализаторов разложения в комплексную форму?deps писал(а):3.Оправдано ли применение перекиси или другого окислителя? ...
Коричневая окраска появлялась, когда присутствовал восстановитель, в частности Fe(+2), а здесь его уже не было к моменту внесения.deps писал(а):УМолибдат,ванадат-никаких изменений (раньше,как Вы помните,проявлялась интенсивно коричневая окраска при его внесении).
Успехов
Бог на стороне не больших батальонов, а тех, кто лучше стреляет (приписывается Вольтеру)
Re: Хелат железа
Ув.amik,спасибо за быстрый комментарий,теперь к Вам практический вопрос.
дабы избежать этого нежелательного избытка,сколько нужно взять 3% расствора перекиси для окисления 3.58 г/л железного купороса (0.7 г/л по железу) и восстановления 0.24 г/л медного (0.06 г/л по меди) в 1 л воды?Или можно применить какой-нибудь другой окислитель? Можно ли заменить медный купорос на нитрат меди 3х водный?Спасибо.возможный небольшой избыток перекиси
Re: Хелат железа
На медь, как таковую, перекись не нужна т.к. окисляется все-таки железо.
Посчитать просто. Одна молекула перекиси водорода может окислить 2 молекулы сульфата железа или 34 грамма 100% H2O2 окислят(теоретически) 2*278 грамма купороса. На 3,58г тогда нужно 0,22 г чистой перекиси или 0,22*100/3=7,33 г разбавленной 3%-ой. Взять лучше с небольшим избытком, ибо при хранении идет медленное, но неотвратимое падение концентрации H2O2 в растворе.
Медный купорос на нитрат меди заменить можно. Меди, как понимаю, вводится немного относительно основного микроэлемента и нитрат-ион в этом случае не повредит.
Посчитать просто. Одна молекула перекиси водорода может окислить 2 молекулы сульфата железа или 34 грамма 100% H2O2 окислят(теоретически) 2*278 грамма купороса. На 3,58г тогда нужно 0,22 г чистой перекиси или 0,22*100/3=7,33 г разбавленной 3%-ой. Взять лучше с небольшим избытком, ибо при хранении идет медленное, но неотвратимое падение концентрации H2O2 в растворе.
Медный купорос на нитрат меди заменить можно. Меди, как понимаю, вводится немного относительно основного микроэлемента и нитрат-ион в этом случае не повредит.
Бог на стороне не больших батальонов, а тех, кто лучше стреляет (приписывается Вольтеру)
Re: Хелат железа
После долгих поисков и экспериментов,наконец-то получил (вобще-то давненько,но сейчас с более детальными корректировками,благодаря Вашим ценным советам) состав пит.расствора железа и ОЭДФ,а также другими микроэлементами.Но,как известно,охота-пуще неволи,решил возобновить работу над составом комплекса Fe-НТФ и комплексом других микроэлементов.Опираясь на статью,которую предоставил ув.amik ,учитывая предыдущие проблемы приведшие к фиаско,начал эксперименты.Много было унитазировано и перебито,но в конце концов получил пит. расствор железа и НТФ, а также комплекса ряда биологически важных микроэлементов.
К рассмотрению предложу основные металлы,следовые опустим.Указание в статье на получение расстворимого комплекса железа-НТФ при РН 6-8,на практике,лично у меня не подтвердилось.Расстворимый комплекс получил при РН-9,нейтрализация проводилась гидрокарбонатом калия с РН 2.5 до РН 9.Изначально,внеся навеску железоаммонийных квасцов(в будущем заменю на сульфат железа) в среду НТФ,наблюдалось молочно-белое хлопьевидное окрашивание расствора (аналогично поведению с ОЭДФ),РН-2.5,при постоянном перемешивании,добавлял карбокислый калий,при РН 8-8.5,расствор начал обесцвечиваться,а к 9-абсолютно стал прозрачным,без признаков осадочных явлений,светло-салатового цвета,т.е как и раньше-монохелат железа при РН,но не 11,а 9.Следующей солью был хлорид марганца,вспоминая раннее отрицательный эффект очень боялся этого,что и получил-опять хлопья,помутнение ит.д.Сидя в раздумьях и созерцая колбу с суспензией,по началу не знал что делать,потом вспомнил,что amik советовал прогревать расствор,поставил на прогрев и...результат не заставил долго ждать-расствор обесцветился,стал прозрачный слегка с коричневым оттенком.Следующее внесение сульфата меди-опять мандраж,те же хлопья,прогрев и перемешивание-всё идеально становилось на свои места.После меди следующее внесение солей-цинка,кобальта,никеля,молибдена,ванадия-прогрев и перемешивание ликвидировало все осадочные явления.В последнюю очередь была внесена борная кислота и сульфат магния,РН расствора-7.5,добавил немного серной кислоты,и понизил до нейтральных значений-6.8-7.0.Расствор темновато-зелёного цвета,без намёка на осадки и прочая.
Начал вносить в аквариум с большой биомассой живых растений,где до этого применялся комплекс железо+ОЭДФ,третья неделя-полёт нормальный,растения нормально реагируют,окрашиваются и не наблюдается недостатка какого то либо элемента.Т.е можно предположить о создании комлекса на НТФ и его практическом применении.Радость открытия омрачается совершенно другим фактором-это избыток силикатов в водопроводной воде,но это уже другая тема viewtopic.php?f=4&t=100111.Ув.[b]amik [/b],я думаю Вам будет интересно моё изложение,не проходите мимо,подкорректируйте мои действия,Ваши советы для меня-эта та база с которой начинаю творить.Спасибо.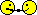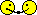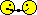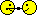
К рассмотрению предложу основные металлы,следовые опустим.Указание в статье на получение расстворимого комплекса железа-НТФ при РН 6-8,на практике,лично у меня не подтвердилось.Расстворимый комплекс получил при РН-9,нейтрализация проводилась гидрокарбонатом калия с РН 2.5 до РН 9.Изначально,внеся навеску железоаммонийных квасцов(в будущем заменю на сульфат железа) в среду НТФ,наблюдалось молочно-белое хлопьевидное окрашивание расствора (аналогично поведению с ОЭДФ),РН-2.5,при постоянном перемешивании,добавлял карбокислый калий,при РН 8-8.5,расствор начал обесцвечиваться,а к 9-абсолютно стал прозрачным,без признаков осадочных явлений,светло-салатового цвета,т.е как и раньше-монохелат железа при РН,но не 11,а 9.Следующей солью был хлорид марганца,вспоминая раннее отрицательный эффект очень боялся этого,что и получил-опять хлопья,помутнение ит.д.Сидя в раздумьях и созерцая колбу с суспензией,по началу не знал что делать,потом вспомнил,что amik советовал прогревать расствор,поставил на прогрев и...результат не заставил долго ждать-расствор обесцветился,стал прозрачный слегка с коричневым оттенком.Следующее внесение сульфата меди-опять мандраж,те же хлопья,прогрев и перемешивание-всё идеально становилось на свои места.После меди следующее внесение солей-цинка,кобальта,никеля,молибдена,ванадия-прогрев и перемешивание ликвидировало все осадочные явления.В последнюю очередь была внесена борная кислота и сульфат магния,РН расствора-7.5,добавил немного серной кислоты,и понизил до нейтральных значений-6.8-7.0.Расствор темновато-зелёного цвета,без намёка на осадки и прочая.
Начал вносить в аквариум с большой биомассой живых растений,где до этого применялся комплекс железо+ОЭДФ,третья неделя-полёт нормальный,растения нормально реагируют,окрашиваются и не наблюдается недостатка какого то либо элемента.Т.е можно предположить о создании комлекса на НТФ и его практическом применении.Радость открытия омрачается совершенно другим фактором-это избыток силикатов в водопроводной воде,но это уже другая тема viewtopic.php?f=4&t=100111.Ув.[b]amik [/b],я думаю Вам будет интересно моё изложение,не проходите мимо,подкорректируйте мои действия,Ваши советы для меня-эта та база с которой начинаю творить.Спасибо.
Re: Хелат железа
И вот ещё такая статья есть про железо и ОЭДФ.http://vestnik.udsu.ru/2012/2012-044/vuu_12_044_10.pdf
Re: Хелат железа
Коллега deps, кажется мне, что Вы теперь сами дадите консультацию любому профи в практической работе 
Не пробовали вести добавление сразу в горячий раствор, естественно при перемешивании? Последовательное внесение отдельных добавок солей металлов с промежуточным охлаждением реакционной смеси (если я правильно понял) оказывается весьма длительным и немного напоминает древнюю алхимическую кухню для посвященных Думаю, что в Ваших интересах сократить время процесса приготовления питательного раствора, но не в ущерб качеству.
Думаю, что в Ваших интересах сократить время процесса приготовления питательного раствора, но не в ущерб качеству.
Не пробовали вести добавление сразу в горячий раствор, естественно при перемешивании? Последовательное внесение отдельных добавок солей металлов с промежуточным охлаждением реакционной смеси (если я правильно понял) оказывается весьма длительным и немного напоминает древнюю алхимическую кухню для посвященных
Бог на стороне не больших батальонов, а тех, кто лучше стреляет (приписывается Вольтеру)
Re: Хелат железа
ув.amik,дело в том,что изначально температура дистиллята порядка 60-70 градусов,перемешивание конечно постоянное,но заготовки навесок регентов занимают небольшое,но всё таки время и расствор немного остывает,а осадки исчезают при прогреве практически до точки кипения.Вот поэтому и приходится прогевать заново после внесения очередной соли.Разживусь эл.-магн.мешалкой,думаю будет легче.Не пробовали вести добавление сразу в горячий раствор, естественно при перемешивании?
Re: Хелат железа
Тогда можно заранее приготовить про запас крепкие растворы с известной концентрацией всех нужных солей и дозировать заданное количество пипеткой. Так будет быстрее и не менее надежно, чем каждый раз брать десяток навесок.
Бог на стороне не больших батальонов, а тех, кто лучше стреляет (приписывается Вольтеру)
Re: Хелат железа
Очень неплохой вариант,спасибо.Ув.amik ,возвращаясь к истокам,посоветуйте пожалуйста нейтрализующий агент,чтобы не привносил большое кол-во калия,т.к этот макроэлемент вноситься отдельно,и аммоний,т.к при РН аквариумной более 7.5 он проявляет токсичность,да и с квасцами уже поступает. 
Re: Хелат железа
В данном случае только сода или NaOH т.е. в составе будет балластный натрий вместо калия или аммония.
Наверно в идеале растворять в комплексоне заранее осажденные и промытые гидроксиды металлов, в первую очередь основной компонент - железо. В таком варианте практически не привносятся посторонние ионы, но это значительно более трудоемко и получится ли вообще
Наверно в идеале растворять в комплексоне заранее осажденные и промытые гидроксиды металлов, в первую очередь основной компонент - железо. В таком варианте практически не привносятся посторонние ионы, но это значительно более трудоемко и получится ли вообще
Бог на стороне не больших батальонов, а тех, кто лучше стреляет (приписывается Вольтеру)
Re: Хелат железа
Спасибо большое за ответы и советы,буду нейтрализовывать солями калия(гидрокарбонат,цитрат,тартрат и т.д),чем солями аммония.Просто при расчёте калийной подкормки учитывать количество поступившего калия с нейтрализатором. 
Re: Хелат железа
Доброе утро.Разобравшись с поведением меди при изготовлении пит.растворов на ОЭДФ с солями железа 2,т.е её восстановление до 1+,затем окисление перекисью Fe2+ в Fe3+,получив безосадочный раствор, вдруг возник вопрос о применении окислителя,как альтернативный вариант перекиси водорода. 
Возможно ли применить в качестве окислителя калий марганцевокислый (КМnО4),при этом "убив двух зайцев",т.е и окислитель и источник марганца,количество перманганата взять из расчёта необходимого по катиону Мn2+? Спасибо.
Спасибо.
Возможно ли применить в качестве окислителя калий марганцевокислый (КМnО4),при этом "убив двух зайцев",т.е и окислитель и источник марганца,количество перманганата взять из расчёта необходимого по катиону Мn2+?
Re: Хелат железа
Вот небольшой фотоотчёт о применении перманганата калия вместо перекиси водорода.Кол-во КМnO4 было взято из расчёта 0.4 г/л по Мn (1,15 г/л).
1-й этап:в среду ОЭДФ внесён FeSO4*7H2O,затем соли Zn,Сu,Mg,Co,Mo,V,Ni,Rb,Cs,H3BO3,а также микродозы солеЙ РЗЭ,раствор темновато-жёлтого цвета,РН-3.4. 2-й этап:нейтрализация расствора цитратом калия 3-зам.до РН 6.Раствор кирпично-бурого цвета. 3-й этап:внесение перманганата калия. А теперь окончательный вариант питательного раствора после постоянного 15 минутного перемешивания с прогревом.
1-й этап:в среду ОЭДФ внесён FeSO4*7H2O,затем соли Zn,Сu,Mg,Co,Mo,V,Ni,Rb,Cs,H3BO3,а также микродозы солеЙ РЗЭ,раствор темновато-жёлтого цвета,РН-3.4. 2-й этап:нейтрализация расствора цитратом калия 3-зам.до РН 6.Раствор кирпично-бурого цвета. 3-й этап:внесение перманганата калия. А теперь окончательный вариант питательного раствора после постоянного 15 минутного перемешивания с прогревом.
У вас нет необходимых прав для просмотра вложений в этом сообщении.
Re: Хелат железа
Да,жаль,amikа нет и прокомментировать никто не хочет. 

Кто сейчас на конференции
Сейчас этот форум просматривают: нет зарегистрированных пользователей и 15 гостей